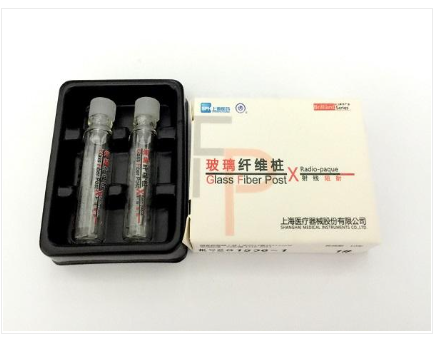
本文轉(zhuǎn)自:浙江日?qǐng)?bào)
國(guó)辦印發(fā)意見(jiàn)
全面深化藥品醫(yī)療器械監(jiān)管改革
據(jù)新華社北京1月3日電 國(guó)務(wù)院辦公廳日前印發(fā)《關(guān)于全面深化藥品醫(yī)療器械監(jiān)管改革促進(jìn)醫(yī)藥產(chǎn)業(yè)高質(zhì)量發(fā)展的意見(jiàn)》(以下簡(jiǎn)稱《意見(jiàn)》)。
《意見(jiàn)》明確5方面24條改革舉措。一是加大對(duì)藥品醫(yī)療器械研發(fā)創(chuàng)新的支持力度。完善審評(píng)審批機(jī)制全力支持重大創(chuàng)新,加大中藥研發(fā)創(chuàng)新支持力度,發(fā)揮標(biāo)準(zhǔn)對(duì)藥品醫(yī)療器械創(chuàng)新的引領(lǐng)作用,完善藥品醫(yī)療器械知識(shí)產(chǎn)權(quán)保護(hù)相關(guān)制度,積極支持創(chuàng)新藥和醫(yī)療器械推廣使用。二是提高藥品醫(yī)療器械審評(píng)審批質(zhì)效。加強(qiáng)藥品醫(yī)療器械注冊(cè)申報(bào)前置指導(dǎo),加快臨床急需藥品醫(yī)療器械審批上市,優(yōu)化臨床試驗(yàn)審評(píng)審批機(jī)制、藥品補(bǔ)充申請(qǐng)審評(píng)審批和藥品醫(yī)療器械注冊(cè)檢驗(yàn),加快罕見(jiàn)病用藥品醫(yī)療器械審評(píng)審批。三是以高效嚴(yán)格監(jiān)管提升醫(yī)藥產(chǎn)業(yè)合規(guī)水平。推進(jìn)生物制品(疫苗)批簽發(fā)授權(quán),促進(jìn)仿制藥質(zhì)量提升,推動(dòng)醫(yī)藥企業(yè)生產(chǎn)檢驗(yàn)過(guò)程信息化,提高藥品醫(yī)療器械監(jiān)督檢查效率,強(qiáng)化創(chuàng)新藥和醫(yī)療器械警戒工作,提升醫(yī)藥流通新業(yè)態(tài)監(jiān)管質(zhì)效。四是支持醫(yī)藥產(chǎn)業(yè)擴(kuò)大對(duì)外開(kāi)放合作。深入推進(jìn)國(guó)際通用監(jiān)管規(guī)則轉(zhuǎn)化實(shí)施,探索生物制品分段生產(chǎn)模式,優(yōu)化藥品醫(yī)療器械進(jìn)口審批,支持藥品醫(yī)療器械出口貿(mào)易。五是構(gòu)建適應(yīng)產(chǎn)業(yè)發(fā)展和安全需要的監(jiān)管體系。持續(xù)加強(qiáng)監(jiān)管能力建設(shè),大力發(fā)展藥品監(jiān)管科學(xué),加強(qiáng)監(jiān)管信息化建設(shè)。
注:文章來(lái)源于網(wǎng)絡(luò),如有侵權(quán),請(qǐng)聯(lián)系刪除





 全部商品分類
全部商品分類